EDITORIAS

studo com proteína do veneno da jararaca revela que a flexibilidade e interações superficiais são fundamentais para a função das proteínas e para a regulação celular
Pesquisadores da Universidade Federal do Rio de Janeiro (UFRJ) descobriram que a proteína jarastatina, presente no veneno da jararaca (Bothrops jararaca), desafia conceitos clássicos da biologia molecular e revela um mecanismo inovador de funcionamento das proteínas dentro das células. O estudo foi publicado na plataforma The Conversation Brasil pelos cientistas Fabio C. L. Almeida, Aarão Camilo Ramos, Ariana Azevedo Vasconcelos e Larissa Saraiva da Silva Santos.
A proteína, chamada jarastatina, desafia uma regra clássica da biologia: ao contrário da maioria das proteínas, que escondem partes que não gostam de água no seu interior, a jarastatina mantém essas regiões expostas na superfície. Surpreendentemente, isso não a torna instável pelo contrário: ela é extremamente solúvel, estável e funcional mesmo dentro de células cheias de outras moléculas.
“À primeira vista, deveria se desmanchar na água, mas a jarastatina é como um super-herói das proteínas. Ela se mantém firme e cumpre seu papel com perfeição”, explica Fabio C. L. Almeida, um dos pesquisadores da UFRJ.
Veja também

Estudo aponta que genética pode influenciar quando o autismo é diagnosticado
Descoberta congelante: HPV é encontrado em múmias de 45 mil anos e muda história da doença
PROTEÍNAS: PEQUENAS MÁQUINAS ESSENCIAIS PARA A VIDA
As proteínas representam cerca de 15% a 20% do peso total do corpo humano e estão presentes em todas as células. Elas exercem funções fundamentais: estruturais, como nos músculos, pele e cabelos; mensageiras, transmitindo sinais entre células; e catalisadoras, acelerando reações químicas vitais para digestão, respiração e produção de energia.
Para desempenhar essas funções, cada proteína precisa dobrar-se em uma forma tridimensional específica, como uma chave que só funciona se encaixada na fechadura certa. Esse dobramento é controlado por forças químicas, incluindo ligações de hidrogênio e interações entre átomos próximos, além de forças de repulsão que evitam colisões inadequadas.
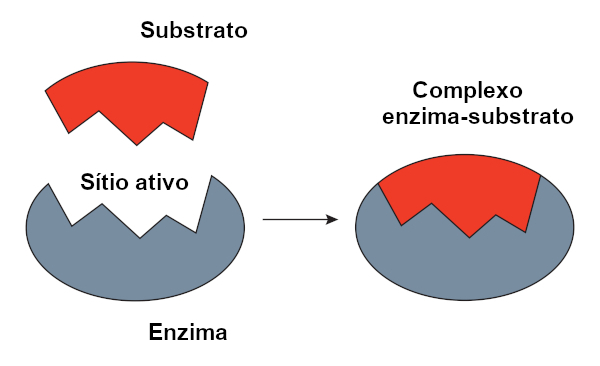
Foto: Reprodução
Em proteínas tradicionais, regiões hidrofóbicas (que “não gostam” de água) se escondem no núcleo da molécula, enquanto regiões hidrofílicas permanecem na superfície, garantindo solubilidade, estabilidade e funcionalidade. Quando o dobramento falha, a proteína pode perder sua função ou interagir de maneira inadequada, levando ao desenvolvimento de diversas doenças.
JARASTATINA: QUEBRANDO TODAS AS REGRAS
A jarastatina se destaca porque suas regiões hidrofóbicas, que normalmente deveriam ficar protegidas no núcleo, estão expostas na superfície da proteína. Inicialmente, isso parece paradoxal: proteínas com hidrofóbicos expostos deveriam ser instáveis e insolúveis em água. No entanto, os pesquisadores observaram que a jarastatina é extremamente estável e altamente solúvel, mesmo em ambientes celulares complexos, que contêm uma mistura intensa de proteínas, carboidratos, ácidos nucleicos e outros compostos.
O PAPEL DOS CLUSTERS HIDROFÓBICOS DE SUPERFÍCIE
Análises detalhadas, realizadas com ressonância magnética nuclear (RMN) e técnicas avançadas como CLEANEX, mostraram que essas regiões hidrofóbicas formam clusters na superfície da proteína. Esses clusters funcionam como pontos de ancoragem fracos, mas altamente eficientes, permitindo que a proteína reconheça e se ligue a diversos alvos, como células do sistema imune, células sanguíneas e até células de câncer de mama.
De forma surpreendente, a água desempenha um papel central nesse mecanismo. Ao redor dos clusters hidrofóbicos, forma-se uma camada de hidratação estruturada, que age como uma blindagem microscópica. Esse arranjo protege as regiões hidrofóbicas, garantindo estabilidade e funcionalidade, mesmo com a exposição aparente à água.
IMPLICAÇÕES PARA A BIOLOGIA CELULAR
Essas descobertas têm implicações profundas. Elas sugerem que interações superficiais transitórias, aparentemente fracas, podem ser tão decisivas quanto estruturas rígidas internas para o funcionamento das proteínas. Os clusters hidrofóbicos de superfície ajudam a formar condensados proteicos, organelas sem membranas que concentram moléculas específicas em locais definidos da célula.
Esses condensados proteicos permitem à célula controlar quando e onde as proteínas se acumulam, regulando processos biológicos com precisão no espaço e no tempo. Em essência, eles funcionam como fábricas microscópicas altamente dinâmicas, coordenando reações bioquímicas essenciais de forma eficiente.
POTENCIAL TERAPÊUTICO DA JARASTATINA
A capacidade da jarastatina de se ligar a diferentes alvos e permanecer funcional em ambientes complexos torna-a um alvo promissor para novos medicamentos. Pesquisas indicam potencial de aplicação em tratamentos de inflamação, trombose e câncer, além de fornecer insights valiosos para o desenvolvimento de proteínas sintéticas com funções específicas.
/i.s3.glbimg.com/v1/AUTH_7d5b9b5029304d27b7ef8a7f28b4d70f/internal_photos/bs/2026/y/t/cWih6vTZyb4Kf8vzhFLQ/file-20260108.jpeg)
Parte hidrofóbica da jarastatina. Imagem gerada pelo
pesquisadores usando o programa de visualizaçãode
estruturas proteicas Pymol (Foto: Divulgação)
Curtiu? Siga o PORTAL DO ZACARIAS no Facebook, Twitter e no Instagram.
Entre no nosso Grupo de WhatApp, Canal e Telegram
O estudo da jarastatina demonstra que a biologia molecular não se limita a regras rígidas de estrutura e dobramento. Flexibilidade, interações transitórias e clusters superficiais podem ser cruciais para a eficiência biológica, revelando como a natureza desenvolveu estratégias sofisticadas para o funcionamento das nanomáquinas da vida.